仕事だけではなく、一般生活の中でもインターネットが身近になり、インターネット(Web)上でのコミュニケーショントラブルが絶えません。
虚偽・誇大な表現を用いた悪質な広告による消費者の被害が増加しています。
そんな広告を取り締まる法律はいくつかありますが、ここ何年かで、それぞれ法改正がなされ、広告表現に関する規制は年々、厳しくなっています。
チェック機関に加えて、競合企業や消費者による連絡も活発化しているので、法を遵守しない安易な広告表現は、企業の信頼を揺るがす危険な行為です。
<知らなかった>では済まされない事態になってきました。
本記事では<知らなかった>リスクを回避するため、「機能性表示食品」の広告制作で<気にすること・押さえること>をお伝えしたいと思います。
目次
「機能性表示食品」とは?
これまで、食品の機能性について表示が認められていたのは、国が個別に許可した「特定保健用食品(トクホ)」と、国の規格基準に適合した「栄養機能食品」だけでした。
それ以外の食品については、その機能について表示することができなかったのです。
例えば、トマトに多く含まれるリコピンには「抗酸化作用がある」とか、青魚に多く含まれるEPA/DHAには「血液をさらさらにする作用がある」といった話を耳にしたことがあると思います。
でも、これまでの表示制度では、特に健康食品やサプリメントにおいて、機能性を謳うことはできず「あいまいな表現でわかりにくい」や「何にいいのか表記されていない」といった不満課題がありました。
そのため、特定保健用食品(トクホ)や栄養機能食品とは異なる、新しい食品の表示制度「機能性表示食品」制度が考えられ、2015年(平成27年)4月1日に施行されました。
「事前届出制」で、
<科学的根拠に基づいた機能性を表示>
食品の「安全性」や「機能性」について一定の条件をクリアする
<事業者の責任>
企業や生産者の責任において「体のどの部分にいいのか」「どう機能するのか」を表示できる
という制度です。
2016年4月からは、機能性表示食品制度の届け出は電子化されました。
実際に届け出るための仕方・提出書類など、詳しくは「機能性表示食品の届出等に関するガイドライン」や消費者庁「機能性表示食品制度届出データベース 」で確認してください。
本記事では、届け出後の販売広告の表示について、を中心にお伝えしたいと思います。
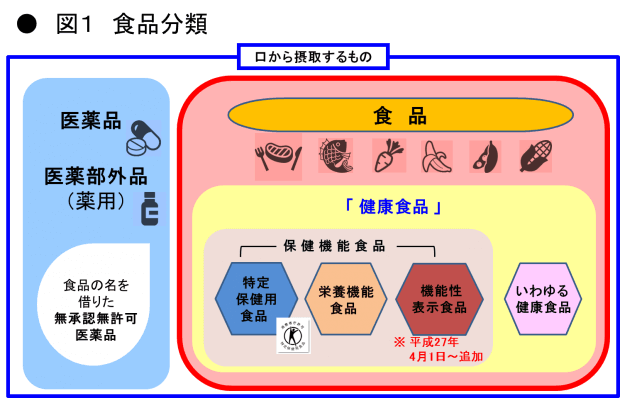
- 食品とされるものの分類をわかりやすく図にすると、下図のようになります。
この分類を踏まえて、以下の記事をみていきましょう。内容の理解に役立つと思います。
「機能性が表示できる食品」って?
ここまでで「機能性表示食品」制度の法律的なことを説明しました。
「この制度、結局のところ、機能性を表示した食品・商品を販売するためにはどうすればいいの?」「ミニ<トクホ>みたいなものですか」と感じている方もいらっしゃると思いますので、少しひも解いて説明しましょう。
今までの食品表示と「機能性表示食品」とで、一番大きく変わる点は?
【今までの食品・健康食品など】
・「医薬品医療機器等法」(旧:薬事法)などの広告法規により、効能効果を謳うことはできなかった。
【新しく追加された機能性表示食品】
・新しい枠組み(保健機能食品)として、機能性(有効性)を表示(謳うこと)することが可能。
ということは、今まで食品・健康食品などで謳えなかった機能性(有効性)は、この制度のルール規定を守れば、謳える(表示できる)ようにしましょう。という点です。
機能性(有効性)を表示するルール規定
以下の3つが該当します。
|
①安全性の確保 ②機能性(有効性)の担保 ③消費者への適切な情報提供 |
つまり、このルールに則らない商品については、”今までどおり、機能性を謳うこと(表示すること)はできません”ということです。
では、新たな機能性表示を広告で行う場合、生鮮食品を含む食品全般を扱う事業者は、どのような点に注意を払う必要があるのでしょうか?
「機能性が表示できる食品」の気にするところ・押さえるところ
対象: 生鮮食品を含めた、すべての食品
基準情報・条件:
1. 疾病に罹患している者、未成年者、妊産婦(妊娠を計画している者を含む。)、
授乳婦を対象としていない食品
2. 機能性の評価となる関与成分が明確で、その機能性についての<科学的な根拠>となる、
届け出た内容が容器包装に表示されている
3. 特別用途食品(特定保健用食品「トクホ」を含む)、栄養機能食品、
アルコールを含有する飲料や脂質、ナトリウムなどの過剰な摂取につながらない食品
4. 食品の安全性と機能性に関する<科学的な根拠>などが、販売日の60日前までに、
消費者庁長官へ必要な事項の届け出*をし、届出番号を受領している
*届け出事項:
a. 食品関連事業者名および連絡先などの食品関連事業者に関する基本情報
b. 安全性及び機能性の科学的な根拠(手法は2つ「臨床試験」または「研究レビュー」)に関する情報
c. 生産・製造及び品質の管理に関する情報
d. 健康被害の情報収集体制に関する情報
e. 容器包装に「機能性表示食品の届出等に関するガイドライン」に基づいて、当該食品に関する表示内容の情報
情報開示と「広告に表示しなければいけない、10項目」
◆表示と情報開示の目的: 消費者の皆さんが誤認することなく、自主的かつ合理的な食品・商品の選択することができるよう、適正な情報提供を行うこと。
★広告(容器包装)に、表示しなければいけない 10項目★
1. 機能性表示食品である旨
2. <科学的な根拠>を有する機能性関与成分および当該成分、
または、当該成分を含有する食品が有する機能性
3. 栄養成分の量および熱量
4. 1日当たりの摂取目安量当たりの機能性関与成分の含有量
5. 1日当たりの摂取目安量
6. 届出番号
7. 食品関連事業者の連絡先
8. 摂取の方法
9. 摂取する上での注意事項
10. 調理又は保存の方法に関し特に注意を必要とするものにあっては当該注意事項
※消費者庁に届け出た後、受理された届け出情報はすべて、消費者庁Webサイトで公開されます。
<科学的な根拠>「研究レビュー」って?
肯定的な結果だけてなく、否定的な結果もすべて合わせて「機能性がある」と認められるかどうかを総合的に判断するものです。「システマティックレビュー」とも呼ばれます。
「研究レビュー」を行う方は、研究論文が登録されているデータベースを用いて、検索キーワードなどの条件をあらかじめ設定し、論文を抽出します。
絞り込まれた論文が、最終製品または機能性関与成分に「機能性がある」と認められるものか?認められていないのか?を分類します。
事業者の都合で、機能性があることを示す論文だけを意図的に抽出することはできません。
★主な注意事項 6つ★
a. 査読付きの研究論文で、機能性が確認されていること
(学会発表の内容だけでは不可/有識者の講演や談話などは不可/
新聞、雑誌などの記事、学説、起源や由来などは不可)
b. 人を対象とした臨床試験や観察研究で、機能性が確認されていること
(動物や細胞レベルの実験では不可/サプリメント形状の食品を
販売しようとする場合は、観察研究は不可)
c. 販売対象とする人と年齢・性別・人種などの観点から、
著しく異なる属性の人だけを対象としていないこと
d. 機能性関与成分に関する研究レビューを行う場合、当該研究レビューに係る成分と
最終製品に含まれる成分の同等性について考察されていること
e. 研究レビューは、信頼性を確保するため、専門知識を持った複数の人で実施すること
f. 著作権法に抵触していないこと
「表現可能な範囲」と「認められない表現」
表現可能な範囲
- 一時的な体調の変化(継続的、慢性的でないもの)で、身体状態を本人が自覚でき、改善に役立つなどの表現
- 容易に測定可能な体調の指標の維持に適する、または改善に役立つなどの表現
⇒OK表現例: 容易に測定可能な体調の指標 = 血圧、体重、体脂肪率 など - 身体の生理機能、組織機能の良好な維持に適する、または、改善に役立つなどの表現
⇒OK表現例: 「目の健康維持に役立つ」「脂肪の吸収をおだやかにします」 など
◎疾病に罹患していない方の健康の維持および増進に役立つ旨の表現。または、適する旨の表現。の表示が可能となります。
※上記の表現可能な範囲内の表示であれば、身体の特定部位に言及した表現も可能となります。
認められない表現
1.「診断」「予防」「治療」「処置」などの医学的な表現
2. 明らかに医薬品と誤認されるおそれのある表現
3. 疾病の治療効果または予防効果を暗示する表現、特定の疾患の方を対象とした表現
⇒ NG表現例:「花粉症に効果あり」「糖尿病の人に」「風邪予防に効果あり」など
4. 健康の維持および増進の範囲を超えた、意図的な健康の増強を標榜するものと認められる表現
⇒ NG表現例: 「肉体改造」「増毛」「美白」など
5. 科学的根拠に基づき説明されていない機能性に関する表現
広告表示関連法規について
冒頭でお伝えしましたが、広告表示に関する規制は年々、厳しくなっています。
広告を取り締まる法律はいくつかありますが、ここ何年かで、それぞれ法改正がなされています。
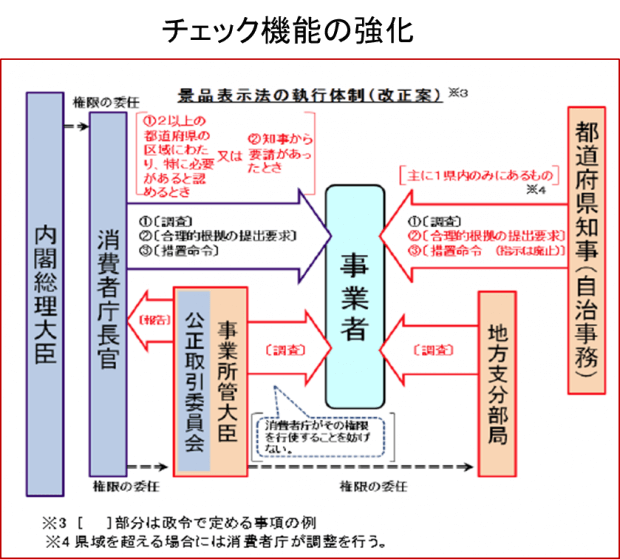
代表的な広告法規の1つに「景品表示法」がありますが、2014年(平成26年)12月1日に改正法が施行されました。
チェック機能の強化(下図参照)がされ、より厳しく摘発・パトロールが活発にされています。
また、この4月1日〔 2016年(平成28年) 〕からは、改正「景品表示法」で追加・検討されていた「課徴金制度」も動き出しました。
「課徴金制度」は、酌量なしの制度なので、「景品表示法」の<注意・排除命令>などのイエローカード・レッドカードというような段階は踏みません。
違反(優良誤認・有利誤認の行為が認定されたら)が見つかれば、いきなりレッドカードです。
これは、事業者は<知らなかった>では済まされないということです。
<このLPは、スグに削除します>、<このサプリの販売はしません>、<二度とやりません>などと、言いわけをしてもダメなのです。
そのほかにも、本記事の主要管轄法規である「医薬品医療機器等法」(旧:薬事法)も、2014年(平成26年)11月25日に改正法が施行され、2015年(平成27年)4月1日には「機能性表示食品」が追加されました。
なお、追加にともない「食品表示法」(食品衛生法、健康増進法、JAS法の食品の表示に関する規定を統合)も新たに施行などなど。
法改正ではありませんが薬事法改正に先駆けて、2013年12月24日には「健康食品ガイドライン」が発表されました。これは「医薬品医療機器等法」(旧:薬事法)+「景品表示法」+「食品表示法」(旧:健康増進法)が範ちゅうになる、厳しいものです。これにより、
⇒1.「根拠データを出せ」など、消費者庁から声のかかるハードルが、きわめて低くなりました。
2. 違反した場合、広告を制作した会社も公表され、罰金も発生します。
また、最近のnews情報によると、特定保健用食品(トクホ)の広告表現の乱れが多くみられ、消費者に誤認を与えているため、厚生労働省など関連省庁は新たに規制する考えとのことです。
ですから、本記事を読んでくださった皆さんが<知らなかった>リスクを理解していただき、企業の信用・信頼を守るために、消費者にわかりやすく・誤解を与えない<法を遵守した>広告制作をしていただくお手伝いになればと思います。
参考
消費者庁「機能性表示食品の届出等に関するガイドライン」
https://www.caa.go.jp/policies/policy/food_labeling/foods_with_function_claims/pdf/foods_with_function_claims_200401_0002.pdf
消費者庁「機能性表示食品制度届出データベース」
http://www.caa.go.jp/policies/policy/food_labeling/foods_with_function_claims/
消費者庁「食品表示基準Q&A」
https://www.pref.ehime.jp/h25300/4793/jigyousha/documents/foods_index_18_170901_0016.pdf
消費者庁「『機能性表示食品』って何?」
https://www.caa.go.jp/policies/policy/food_labeling/about_foods_with_function_claims/pdf/150810_1.pdf
消費者庁「『機能性表示食品制度」が始まります!」
http://www.caa.go.jp/foods/pdf/150810_2.pdf